SRP0407
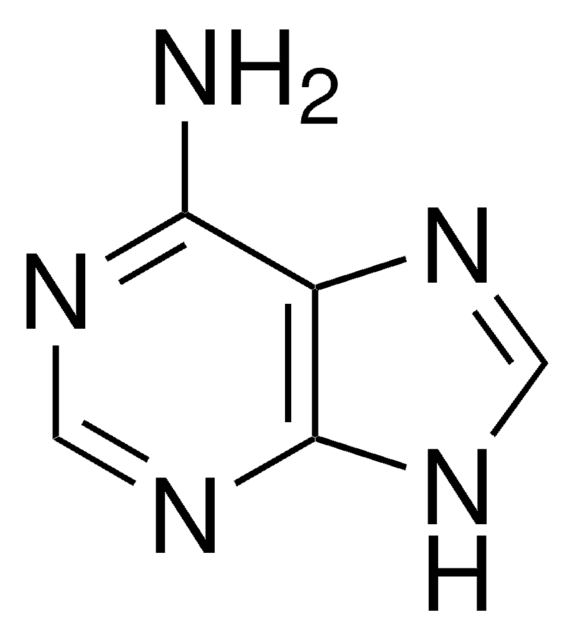
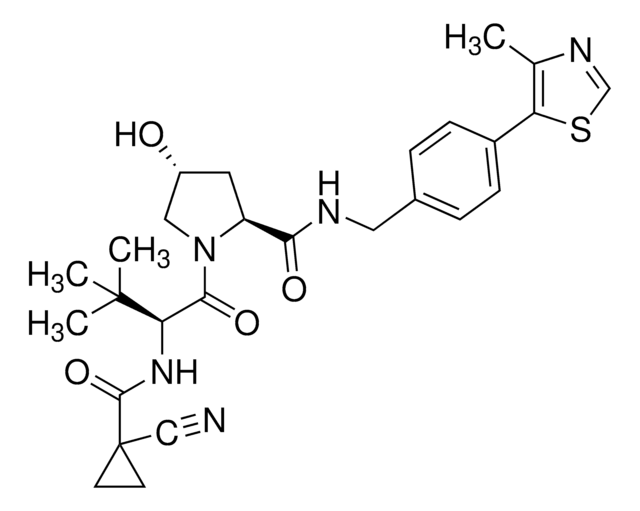
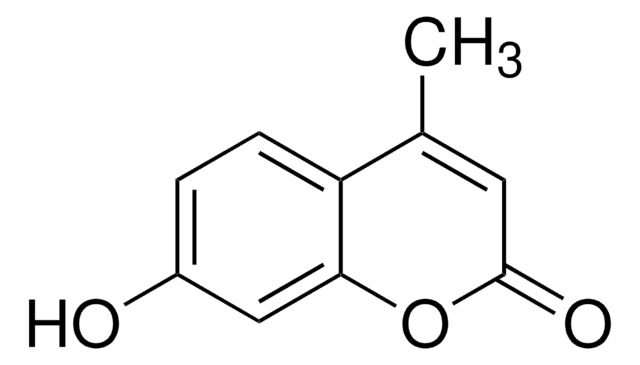
Histone H2b full length human
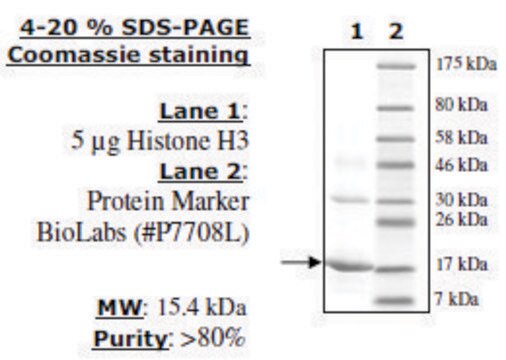
recombinant, expressed in E. coli, ≥65% (SDS-PAGE)
Synonym(e):
H2BFA, histone cluster 1, H2bg
Anmeldenzur Ansicht organisationsspezifischer und vertraglich vereinbarter Preise
Alle Fotos(1)
About This Item
UNSPSC-Code:
12352200
NACRES:
NA.77
Empfohlene Produkte
Biologische Quelle
human
Rekombinant
expressed in E. coli
Assay
≥65% (SDS-PAGE)
Form
aqueous solution
Mol-Gew.
14.6 kDa
Verpackung
pkg of 1 mg
NCBI-Hinterlegungsnummer
UniProt-Hinterlegungsnummer
Versandbedingung
dry ice
Lagertemp.
−70°C
Angaben zum Gen
human ... HIST1H2BG(8339)
WGK
WGK 1
Flammpunkt (°F)
Not applicable
Flammpunkt (°C)
Not applicable
Analysenzertifikate (COA)
Suchen Sie nach Analysenzertifikate (COA), indem Sie die Lot-/Chargennummer des Produkts eingeben. Lot- und Chargennummern sind auf dem Produktetikett hinter den Wörtern ‘Lot’ oder ‘Batch’ (Lot oder Charge) zu finden.
Besitzen Sie dieses Produkt bereits?
In der Dokumentenbibliothek finden Sie die Dokumentation zu den Produkten, die Sie kürzlich erworben haben.
A Comprehensive View of the Epigenetic Landscape Part I: DNA Methylation, Passive and Active DNA Demethylation Pathways and Histone Variants
Anna Sadakierska-Chudy
Neurotoxicity Research, 27 (2015)
Histone H2B ubiquitylation and deubiquitylation in genomic regulation.
N C T Emre et al.
Cold Spring Harbor symposia on quantitative biology, 69, 289-299 (2005-08-25)
Abba Kastin
Handbook of Biologically Active Peptides (2013)
Mary Ann Osley
Briefings in functional genomics & proteomics, 5(3), 179-189 (2006-06-15)
Histone ubiquitylation has emerged as an important chromatin modification with roles in transcription and trans-histone methylation. In the past several years, there has been dramatic progress in the identification of factors that control ubiquitin attachment to the core histones H2A
John J Wyrick et al.
Biochimica et biophysica acta, 1789(1), 37-44 (2008-08-05)
In eukaryotic cells, the genome is packaged with histones H2A, H2B, H3, and H4 to form nucleosomes. Each of the histone proteins is extensively post-translationally modified, particularly in the flexible N-terminal histone tail domains. Curiously, while post-translational modifications in histone
Unser Team von Wissenschaftlern verfügt über Erfahrung in allen Forschungsbereichen einschließlich Life Science, Materialwissenschaften, chemischer Synthese, Chromatographie, Analytik und vielen mehr..
Setzen Sie sich mit dem technischen Dienst in Verbindung.